Das Endocannabinoid-System als Target für Therapie und Diagnostik bei der Alzheimer-Demenz (CanAD)
Forschungsgruppe der Klinik für Psychiatrie und Psychotherapie
Das Endocannabinoid-System ist ein körpereigenes, physiologisches Regulationssystem das evolutionär hochgradig konserviert ist. Das Signalsystem ist an diversen physiologischen Funktionen beteiligt, dazu gehören Gedächtnis, Gehirnentwicklung und Kontrolle der Motorik (Salzet et al. 2000). Eine Modulation des Endocannabinoidsystems eröffnet somit neue therapeutische Möglichkeiten zur Behandlung neurodegenerativer Krankheiten inklusive der Demenz vom Alzheimer-Typ.
Das Endocannabinoid-System besteht aus Cannabinoid-Rezeptoren, ihren endogenen Liganden und Enzymen für Synthese und Abbau der Endocannabinoide. Bislang konnten zwei Cannabinoid-Rezeptortypen identifiziert werden: CB1-Rezeptoren werden vorwiegend von Nervenzellen im ZNS exprimiert, während CB2-Rezeptoren hauptsächlich auf Zellen des Immunsystems oder Organen wie der Milz aber auch auf gehirnständigen Immunzellen, den Mikroglia, lokalisiert sind. Endocannabinoide werden nach Bedarf synthetisiert und spielen eine Rolle bei neuroinflammatorischen Reaktionen im Gehirn, der präsynaptischen Aktivität und haben neuroprotektive und antioxidative Aufgaben im Gehirn (Mechoulam und Parker 2013; Fagan und Campbell 2014). Daher besteht die berechtigte Hoffnung, dass spezifische CB1- oder CB2-Rezeptoragonisten oder -antagonisten, bzw. gezielte Eingriffe in den körpereigenen Endocannabinoid-Stoffwechsel, neue therapeutische Perspektiven für die Alzheimer-Erkrankung eröffnen könnten.
Auswahl aktueller Projekte
Das Endocannabinoid-System als Angriffspunkt für neue Therapieansätze bei der Alzheimer-Erkrankung
In einer aktuellen Studie untersuchen wir den potentiellen Nutzen einer Cannabinoid-basierten Therapie für die Demenz vom Alzheimer-Typ in unterschiedlichen Mausmodellen für diese Erkrankung im Hinblick auf die Beeinflussung der Abeta-Plaque-Pathologie, der Nervenzellverluste, des zerebralen Glucosemetabolismus und der kognitiven Defizite. Zudem ist eine entsprechende klinische Studie in Planung.
Einfluss von Cannabinoiden auf den gesunden Organismus
Neben dem Einsatz von Cannabinoiden als mögliche Therapie für die Alzheimer-Erkrankung beschäftigen wir uns auch mit den Auswirkungen von unterschiedlichen Phytocannabinoiden und synthetischen Cannabinoiden auf den gesunden Organismus. Beispielsweise konnten wir in einer kürzlich veröffentlichten Arbeit zeigen, dass die Langzeitbehandlung mit Cannabidiol keinen negativen Einfluss auf die Gedächtnisleistung und das Angstverhalten von gesunden Mäusen hat (Schleicher et al., 2019).
Wege zu neuen Tracern für die Alzheimer Erkrankung
Eine der ersten Veränderungen und Schlüsselfaktoren der Alzheimer-Erkrankung stellen neuroinflammatorische Prozesse mit der Infiltration aktivierter Mikroglia dar (Krause et al, 2010; Itagaki et al, 1989). Ein vielversprechender Ansatz in der Erfassung der Neuroinflammation ist die Untersuchung des Endocannabinoid-Systems. Der periphere Cannabinoid-Rezeptor CB2 wird unter Normalbedingungen im Gehirn kaum exprimiert, jedoch bei neuroinflammatorischen oder neurodegenerativen Prozessen vor allem in den Mikroglia deutlich hochreguliert. Histopathologisch konnte gezeigt werden, dass CB2-Rezeptoren in Gehirnen von Patient*innen mit Morbus Alzheimer stark hochreguliert sind (Benito et al. 2003; Solas et al. 2012). Daher stellt CB2 eine ideale Zielstruktur für die nicht-invasiven Diagnostik der Demenz vom Alzheimer-Typ dar.
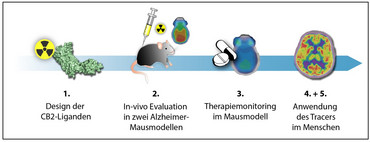
Das Ziel dieses Projekts ist die Entwicklung neuer radioaktiver Tracer zur Darstellung der CB2-Expression in Gehirn von Patient*innen mit Demenz vom Alzheimer-Typ mittels Positronen-Emissions-Tomographie (PET). Mit Hilfe dieser PET-Tracer sollen Patient*innen mit dem Verdacht einer Demenz zu einem möglichst frühen Zeitpunkt diagnostiziert werden.
Geeignete CB2-Liganden mit einer hohen Affinität und Selektivität für den CB2-Rezeptor werden radioaktiv markiert und zunächst in verschiedenen Mausmodellen für die Demenz vom Alzheimer-Typ evaluiert. Dabei wird insbesondere untersuch ab wann prä-symptomatische Veränderungen im Gehirn der Tiere zu detektieren sind. Zudem sollen mittels CB2-PET/CT Therapieerfolge im Mausmodell schon im Verlauf therapeutischer Maßnahmen überprüft werden.
Kollaborationen
Intern: Priv.-Doz. Dr. Caroline Bouter, Oberärztin, Klinik für Nuklearmedizin
Extern: Dr. Nicola Beindorff, Leitung Berlin Experimental Radionuclide Imaging Center (BERIC), Charité Berlin
Kontakt
Leitung
Kontaktinformationen
- Telefon: +49 551 3965248
- E-Mail-Adresse: yvonne.bouter(at)med.uni-goettingen.de
Das könnte Sie auch interessieren